|
|
碘化钠 |
| CAS No.: |
7681-82-5 |
| 分子式: |
NaI |
| 分子量: |
149.89 |
| 备注: |
中文名称碘化钠中文同义词碘化钠无水;无水碘化钠;水合碘化钠;超干碘化钠;碘化鈉;碘化钠,无水;无水碘化钠(99+%);碘化钠,超干,99.99%(METALSBASIS)英文名称Sodiumiodide英文同义词SODIUMIODIDE;UV-VISSTANDARD3;UV-VISSTANDARD3:SODIUMIODIDE;Anayodin;Hydriodicacidsodiumsalt;ioduredesodium;Ioduril;JodidsodnyCAS号7681-82-5分子式NaI分子量149.89EINECS号231-679-3相关类别催化和无机化学;无机化合物;医药中间体;通用试剂;轻金属;精细化工;化工原料;无机化工原料;碘化物系列;化工产品-有机化工;生化试剂-其他化学试剂;无机化工;无机盐;Ci碘;无机化工产品;标准品和标准物质;专业试剂;无机化合物和盐;生化试剂;钠;合成材料中间体;基础原料;大化工;中间体类;医药原料药;化工;化工材料;精细化工原料;医药原料;食品添加剂;原料;抗病毒类中间体;通用生化试剂-无机盐;系列1;卤素化合物;碘化物系列碘化物系列;Inorganics;EssentialChemicals;ReagentPlus;RoutineReagents;InorganicSalts;SyntheticReagents;Pharmacopoeia(USP);PharmacopoeiaA-ZPharmacopoeia(USP);PharmacopoeialInorganics;CrystalGradeInorganics;Salts;SodiumSalts;SodiumMetalandCeramicScience;ACSGradeSyntheticReagents;MetalandCeramicScience;AnalyticalReagentsforGeneralUse;Purissp.a.;Q-S,Purissp.a.;metalhalide;ChemicalSynthesis;CrystalGradeInorganics;InorganicSalts;MaterialsScience;MetalandCeramicScience;Sodium;SodiumSalts;SyntheticReagents;Ultra-HighPurityMaterials;Auxiliaries;化学试剂;bc0001Mol文件7681-82-5.mol结构式碘化钠性质熔点661°C(lit.)沸点1300°C密度3.66蒸气密度>1(vsair)蒸气压1hPa(767°C)折射率1.7745闪点1300-1304°C储存条件Storeat+5°Cto+30°C.溶解度可溶于水形态珠状酸度系数(pKa)0.067[at20℃]颜色白色比重3.67PH值6-9(50g/l,H2O,20℃)水溶解性184g/100mL(25ºC)敏感性HygroscopicMerck14,8631暴露限值ACGIH:TWA0.01ppm介电常数7.2800000000000002稳定性吸湿性InChIKeyFVAUCKIRQBBSSJ-UHFFFAOYSA-MLogP-1.301at25℃CAS数据库7681-82-5(CASDataBaseReference)NIST化学物质信息Sodiumiodide(7681-82-5)EPA化学物质信息Sodiumiodide(7681-82-5)碘化钠用途与合成方法概述碘化钠是由碳酸钠或氢氧化钠与氢碘酸反应,然后蒸发溶液生成的一种白色固体,有无水物、二水合物和五水合物。它用作制碘的原料,用于医学和摄影术。碘化钠的酸性溶液因生成氢碘酸而显示还原性。无水物,化学式NaI。分子量149.89。无色立方晶体或白色粒状物。味咸而稍苦。熔点651℃,沸点1304℃,相对密度3.665(4℃)、3.607(25℃),折光率1.7745。易溶于水(0℃时159.7、20℃时179.3、25℃时184、30℃时190、40℃时205、50℃时227、60℃时257、80℃时296、100℃时302)、乙醇(25℃时43.3)、甲醇(10℃时65.0、25℃时78.0、40℃时80.7、60℃时79、4)、丙酮(20℃时30.0、80℃时21.8)、液氨和吡啶,能溶于甘油中。有强吸湿性。在空气中逐渐吸湿至含水量达5%,可被空气氧化释出碘而变棕色,水溶液呈微碱性,亦有同样变化,可略加碱以使保持稳定。水溶液的pH为8~9.5。应避光密闭保存。晶体为二水合碘化钠,化学式NaI·2H2O,分子量185.92。无色晶体,有潮解性,易溶于水、乙醇和甘油。65℃以上失去结晶水,熔点752℃。有还原性,在空气或水溶液中易被空气中的氧氧化而析出碘颜色变黑。应避光,密封保存。五水合物、二水合物和无水物的转变温度为:NaI·5H2O---(-13.5℃)---NaI·2H2O---(65℃)---NaI碘化钠用做分析试剂、微量分析法测定钯、铂和铊等。碘的助溶剂(碘化钠在水溶液中跟碘形成络合物,增大碘的溶解性),还可用作制药,照相用乳胶和制单晶的原料。应用无水碘化钠是一种白色粉末,化学式为NaI,其用途广泛,利用碘化钠优异的光学性能可与光电倍增管的光阴极很好的配对,制备发光效率很高的光学器件,该光学器件在发光波段没有明显的自吸收,对X射线和γ射线均有良好的分辨能力且温度效应较小。凭借碘化钠的性能和低廉的价格,被广泛的应用于石油探测、安检、环境监测等领域。相关化学反应碘化钠与氯或溴作用,均能生成单质碘,同时能生成卤化钠。(1)2NaI+Cl2=2NaCl+I2(2)2NaI+Br2=2NaBr+I2碘化钠与酸作用,均能生成相应酸的钠盐,同时能生成碘化氢、氢碘酸或单质碘。(3)NaI+H3PO4=NaH2PO4+HI(4)2NaI+H3PO4=NaH2PO4+2HI(5)3NaI+H3PO4=Na3PO4+3HI(6)NaI+H3Sb4=NaH2SbO4(白色)+ChemicalbookHI(7)NaI+H2SO4(浓)=NaHSO4+HI(8)2NaI+3H2SO4(浓)=2NaHSO4+I2+SO2+2H2O(9)NaI+HCl=NaCl+HI碘化钠与次氯酸作用,生成氯化钠、氢氧化钠和单质碘。(10)2NaI+HOCl=NaCl+NaOH+I2碘化钠与下列盐或氧化物作用,能生成不同的钠盐。(11)NaI+6Ce(SO4)2+3H2O=NaIO3+3Ce2(SO4)3+3H2SO4(12)2NaI+4Ce(SO4)2+2HCl=Na2SO4+2Ce2(SO4)2+2ICl+H2SO4(13)NaI+3NaIO4=4NaIO3(14)2NaI+3NaIO4+3H2O=NaIO3+2Na2H3IO6+I2(15)2NaI+2CO2+H2O2=2NaHCO3+I2(16)2NaI+MnO2+3H2SO4=2NaHSO4+MnSO4+I2+2H2O药性与应用用于膀胱造影、逆行尿路造影、经T形管胆道造影及各部位瘘管造影。尿路造影:6.25%100ml。膀胱造影:6.25%150ml。逆行肾盂造影:12.5%5~7ml。T形管胆道造影:12.5%10~30ml。瘘管造影:按病情确定注射部位及剂量。X线造影剂毒性较大,不可静脉注射。肝、肾功能不全及碘过敏者忌用。用前应做碘过敏试验。注意与禁忌X线造影剂是利用X线易透过或不易透过的性质作为对比,使被检部位显影的药物。目前临床上使用的造影剂,分为阴性造影剂(显影密度低于人体软组织)和阳性造影剂(显影密度高于人体软组织)两类。阴性造影剂有空气、二氧化碳及氧气等。阳性造影剂除硫酸钡外,几乎均为碘化物和有机碘化合物。碘化钠最早应用于泌尿系统造影。有机碘化合物中的碘碳键相当稳固,不易形成碘离子,对人体几无生理作用。X线造影剂在机体某些器官或组织中经吸收和适当集中后,达到一定浓度时,能吸收X线,可供造影之用。它们可分为水溶性和油溶性两种,根据化学类型不同,前者可分为酞类、有机酸类、磺酸类和吡啶酮类;后者主要为碘化油类。理想的造影剂应具备下列要求:显影清晰;无毒性、无不良反应;易于吸收和排泄;理化性质稳定,能久贮不变质;使用简便;制造方便,价格低廉。水中溶解度(g/100ml)不同温度(℃)时每100毫升水中的溶解克数:159g/0℃;167g/10℃;178g/20℃;191g/30℃;205g/40℃257g/60℃;295g/80℃;302g/100℃合成工艺(1)称取200公斤碘,250公斤碳酸氢钠,将其混合后置于200公斤的水中,充分搅拌得到混合溶液一;(2)在混合溶液一中加入24公斤水合肼,混合均匀后得到混合溶液二;(3)将混合溶液二在50℃温度下反应1h,得到pH为6.5的混合溶液三;(4)在混合溶液三中加入氢氧化钠溶液,调整混合溶液pH值至9后,在100℃下保温8h,得到混合溶液四;(5)在混合溶液四中加入HI溶液,调整混合溶液的pH至3,在75℃下保温4h;(6)在步骤(5)保温结束后的溶液中加入氢氧化钠溶液,调整混合溶液的pH至6.5,即制得粗NaI溶液;(7)在制得的粗NaI溶液中加入活性炭0.4公斤,混合均匀后静置24h后过滤除杂,并将滤液经减压蒸馏后得到浓缩溶液,减压蒸馏的压力为-0.5MPa,蒸馏温度为80℃;(8)将浓缩溶液经离心分离除去液体,将固体干燥后得到碘化钠粉体;(9)将干燥后的碘化钠粉体置于无水酒精中进行重结晶提纯,干燥后制得本发明的高纯无水碘化钠粉体。经检测,制备的无水碘化钠的纯度为99.9%,其中杂质K的含量为1.5ppm,松装密度为2.44g/mL。毒性参见碘。化学性质无色立方晶体或白色结晶性粉末。无臭、味咸苦。易溶于水,溶于甲醇、乙醇、丙酮、甘油、液氨和液体二氧化硫。水溶液呈微碱性。用途用作分析试剂和碘的助溶剂,也用于制药工业用途用作分析试剂和制备单晶的原料用途用作制备各类碘化合物的原料,也用于医药、照相等用途是制造无机碘化物和有机碘化物的原料。在医药上用作祛痰剂和利尿剂,也用于治疗甲状腺肿病。可用作照相胶片感光剂,碘的助溶剂,也用于配制碘乳剂。用途用于微量测定铯、铂和铊等用途化学工业用作制备无机和有机碘化物的重要原料,也用作碘的助溶剂和用于配制碘乳剂。医药工业用于生产祛痰剂和利尿剂等药物。感光工业用作胶片的感光剂,分析化学中用作点滴分析及其他分析试剂。化学反应中用作氧化剂。当温度低于65.6℃,碘化钠在水溶液中形成含水数目不定的各种水合物。室温下由溶液析出二水物,为无色棱形晶体,-13.5~31.5℃内可析出五水物。与二氧化硫作用,生成相应的稳定化合物。有还原性,可被氧化别氧化,游离出碘。生产方法八碘化三铁法按碘:铁屑=3.3:1的质量比,先将洗净的铁屑加入反应器内,再加水,加水量与铁屑质量比为7:1。分批加入碘片,由于碘和铁反应时产生大量的热,在反应器外需用冷水冷却,使其温度低于65℃。加入碘片后溶液呈深红棕色,待溶液呈淡绿色后,加入第二批碘,过滤除去铁屑,再加入碘反应生成八碘化三铁。在容器中加入碳酸氢钠溶液,在搅拌下缓慢加入八碘化三铁进行反应,此时有二氧化碳气体逸出。反应溶液经静置,吸出上层清液,蒸发浓缩至70~72°Bé,趁热过滤,经冷却结晶、离心分离、干燥,制得碘化钠成品。其Fe+I2→FeI23FeI2+I2→Fe3I8Fe3I8+8NaHCO3→8NaI+Fe3O4+4H2O+8CO2↑铁屑还原法取理论量的:100%~103%烧碱,加水稀释成10%溶液,于反应器中加热至60~80℃,在搅拌下分次加入定量碘,于80~90℃保温搅拌反应约1h,反应液为棕色,Ph值为6~7,同时有碘酸钠的白色结晶析出。将反应液降温至30℃以下,加入2倍于理论量的铁屑使碘酸钠还原成碘化钠。开始反应较剧烈,待反应缓和后,加热煮沸,继续搅拌反应1~2h,然后用10%烧碱溶液调节Ph值为8,煮沸30min,经冷却、静置过滤,将无色透明滤液蒸发浓缩、析出结晶,再趁热过滤、干燥,制得碘化钠成品。其3I2+6NaOH→5NaI+NaIO3+3H2ONaIO3+3Fe+3H2O→NaI+3Fe(OH)2 |
| 结构式: |
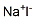 |
 |
|
声明:以上信息未经本网证实,仅供参考,华夏化工网不承担任何风险责任. |
|