|
|
氯化锆 |
| CAS No.: |
10026-11-6 |
| 分子式: |
ZrCl4 |
| 分子量: |
233.02 |
| 备注: |
中文名称氯化锆中文同义词无水四氯化锆;氯化锆(IV),98%,CONT.1-2%HAFNIUM(IV)CHLORIDE;氯化锆(IV),REACTORGRADE,99.5+%(METALSBASIS);氯化锆(IV);氯化锆(IV),REACTORGRADE(METALSBASIS);无水氯化锆;氯化锆(IV),无水,98%;氯化鋯英文名称Zirconiumtetrachloride英文同义词(beta-4)-zirconiumchloride(zrcl4;(T-4)-Zirconiumchloride;tetrachlorozirconium;tetra-zirconiumchlorid;Zirconium(IV)chloride,anhydrous,powder,99.99%metalsbasis;Zirconium(IV)chloride,99.9+%metalsbasis;Zirconium(IV)chloride,99.5+%metalsbasis;ZircomiuntetrachlorideCAS号10026-11-6分子式Cl4Zr分子量233.04EINECS号233-058-2相关类别无机化工;无机卤化物;稀有金属;粉体;锆;氯化物;催化和无机化学;通用试剂;金属卤化物及卤酸盐;金属氯化物及盐;无机盐;有机化工;氨基酸及其衍生物;metalhalide;CatalysisandInorganicChemistry;ChemicalSynthesis;CrystalGradeInorganics;MaterialsScience;MetalandCeramicScience;Salts;Zirconium;ZirconiumSalts;construction;material;工业原料;Chemical;化工-催化剂;无机化工原料;化工原料;有机化工原料;有机贵金属催化剂;高纯材料;无机粉体;精细化工原料;工业化;有机原料Mol文件10026-11-6.mol结构式氯化锆性质熔点437°C沸点331°C密度2.8g/mLat25°C(lit.)蒸气压1mmHg(190°C)储存条件Storebelow+30°C.溶解度易溶于乙醇、乙醚、盐酸。形态粉末颜色白色比重2.803PH值<1(H2O,20℃)(saturatedaqueoussolution)水溶解性Reactswithwater.敏感性MoistureSensitive&Hygroscopic水解敏感性7:reactsslowlywithmoisture/water晶系MonoclinicMerck14,10174空间群P2/c晶格常数a/nmb/nmc/nmα/oβ/oγ/oV/nm30.6360.7410.62690109.3900.2782暴露限值ACGIH:TWA5mg/m3;STEL10mg/m3NIOSH:IDLH25mg/m3;TWA5mg/m3;STEL10mg/m3CChemicalbookAS数据库10026-11-6(CASDataBaseReference)NIST化学物质信息Zirconiumtetrachloride(10026-11-6)EPA化学物质信息Zirconiumtetrachloride(10026-11-6)氯化锆用途与合成方法理化性质氯化锆又称四氯化锆,一种常见锆化合物,化学式ZrCl4。分子量233.03。白色有光泽的结晶或粉末。熔点4.37℃(2.53×106Pa),相对密度2.80315。331℃升华。其气体分子为单体,具有正四面体结构,其固态互相缔合组成以ZrCl6八面体为单元的锯齿形链状结构。在潮湿空气中产生盐酸烟雾,遇水强烈水解生成氯化氧锆。可与氯化物、醚、酯等分子加合形成六配位的配合物。吸收氨形成氨复盐ZrCl4·4NH3,与五氯化磷作用形成磷复盐2ZrCl4·PCl5。结构与四氯化钛不同,固态的ZrCl4中存在着以锆原子为中心的含有氯桥连接的八面体配位结构。这也就解释了它们在熔点上的巨大差异。这种结构还出现在HfCl4中。当使用路易斯碱进行处理时,Zr-Cl-Zr形式的氯桥会断裂,从而使聚合物分解。例如,四氯化锆可以和含羟基的配体发生氯置换反应,和水反应可生成ZrOCl2。用途四氯化锆是一种弱的路易斯酸,能与五氯化磷形成加合物ZrCl4·PCl5和ZrCl4·2PCl5,或和碱金属或碱土金属氯化物形成六氯锆酸盐。此外,它还可以代替三氯化铝参与傅-克反应和狄尔斯–阿尔德反应。四氯化锆是用于对二氧化锆和二硼化锆进行化学气相沉积的最重要的前体。它还被用作纺织品防水剂、皮革鞣剂、分析试剂。制备四氯化锆可由氯气与碳化锆(或二氧化锆与碳的混合物)反应制备,再用升华法提纯。健康危害氯化锆吸入后会引起呼吸道刺激。对眼有强烈刺激性。皮肤直接接触液体有强烈刺激性,可致灼伤。口服出现口腔和咽喉烧灼感、恶心、呕吐、水样便、血便、虚脱和惊厥。慢性影响:右引起皮肤肉芽肿。对呼吸道有轻度刺激作用。危险特性:受热或遇水分解放热,放出有毒的腐蚀性烟气。用途氯化锆可用于制取金属锆、颜料、纺织品防水剂、皮革鞣剂和分析试剂等。用途用于制取锆化合物和有机金属有机化合物,可作为溶剂和重熔金属镁的净化剂,具有除铁及除硅之功效。生产方法按计量摩尔比称取二氧化锆和煅烧过的炭黑,混合均匀后放入瓷舟。将瓷舟置于瓷管中,在氯气流中加热到500℃进行煅烧。用捕集器在室温下收集产物。考虑到四氯化锆在331℃升华,可用600mm长的管子,在300~350℃于氢气流中将其重新升华,以除去氯化锆中氧化物及三氯化铁。类别腐蚀物品毒性分级中毒急性毒性口服-大鼠LD50:1688毫克/公斤;口服-小鼠LD50:489毫克/公斤可燃性危险特性遇H发孔剂可燃;遇氰化物放出有毒氰化氢气体;受热产生有毒氯化物和含锆化物烟雾储运特性库房通风低温干燥;与氧化剂、氰化物、H发孔剂、碱类分开存放。灭火剂砂土、雾状水、泡沫职业标准TLV-TWA5毫克(锆)/立方米;STEL10毫克(锆)/立方米 |
| 结构式: |
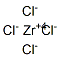 |
 |
|
声明:以上信息未经本网证实,仅供参考,华夏化工网不承担任何风险责任. |
|