|
|
醋酸格拉替雷 |
| CAS No.: |
147245-92-9 |
| 分子式: |
C25H45N5O13 |
| 分子量: |
623.65 |
| 备注: |
中文名称醋酸格拉替雷中文同义词醋酸格拉替雷;格拉替美;醋酸格拉替雷147245-92-9;L-丙氨酸-L-谷氨酸-L-赖氨酸-L-酪氨酸多肽聚合物醋酸盐;格拉替雷-D7;醋酸格卡替雷;L-丙氨酸-L-谷氨酸-L-赖氨酸-L-酪氨酸多肽聚合物醋酸英文名称Glatirameracetate英文同义词GLATIRAMERACETATE;l-glutamicacidpolymerwithl-alanine,l-lysineandl-tyrosine,acetate(salt);511:PN:WO2010103292PAGE:64claiMedsequence;L-AlaninepolyMerwithL-GlutaMicAcidL-LysineL-TyrosineAcetate;L-GlutaMicAcidpeptidewithL-AlanineL-LysineL-TyrosineAcetateSalt;L-TyrosinepolyMerwithL-AlanineL-GlutaMicAcidL-LysineAcetate;ProtiraMer;GaltiraMeracetateCAS号147245-92-9分子式C25H45N5O13分子量623.66EINECS号814-981-5相关类别多肽;原料药;医药原料药;抑制剂;药物多肽;AminoAcids&Derivatives;Intermediates&FineChemicals;Peptides;Pharmaceuticals;APIMol文件147245-92-9.mol结构式醋酸格拉替雷性质熔点>239°C(dec.)储存条件Refrigerator溶解度甲醇(微溶)、水(微溶)形态固体颜色白色至类白色CAS数据库147245-92-9(CASDataBaseReference)醋酸格拉替雷用途与合成方法多肽类药物以色列梯瓦制药公司的拳头产品Copaxone(醋酸格拉替雷)是一种人工合成的肽类制剂,由谷氨酸、丙氨酸、酪氨酸和赖氨酸四种氨基酸组成。Copaxone于1996年获美国FDA核准用于治疗多发性硬化症。在具有较多多发性硬化症患者的西方国家中,Copaxone的疗效与耐受性皆获得十足的肯定。目前国内暂无企业申报格拉替雷或进口。2011年Copaxone全球销售额达到36亿美元。据悉今年一季度,该药物创下了9.09亿美元的销售额。6月,梯瓦制药公司在发布的年度经济预测中表示,该药物今年或将为公司带来高达38亿美元的收入。不过Copaxone可观的收益也引来仿制药公司的挑战。近日,梯瓦制药公司宣布,此前公司同包括Momenta生物制药公司、诺华制药公司山德士分公司、迈兰制药公司以及Natco生物制药公司数家制药公司之间就Copaxone的专利权展开了一场法律诉讼案件,日前美国纽约州法院表示梯瓦制药公司胜诉。梯瓦制药公司对于该药物的市场独家销售权有效期将会延至2014年。市场情况格拉替雷由全球知名公司以色列药厂Teva开发,于1996年获美国FDA核准用于治疗多发性硬化症,目前已在43个主要国家上市。在具有较多多发性硬化症患者的西方国家中,格拉替雷的疗效与耐受性皆获得十足的肯定。2014年12月,以色列制药巨头梯瓦(Teva)又成功开发了长Chemicalbook效版格拉替雷Copaxone用于复发型多发性硬化症(RMS)成人患者的治疗。在美国,Copaxone剂型为40mg/ml,每周注射3次,与每天注射1次普通格拉替雷Copaxone效果相同。据全球畅销药数据显示,该产品2010~2014年普通格拉替雷连续五年销售额超过40.0亿美元以上,市场处于稳定发展阶段。普通格拉替雷Copaxone专利于2015年到期,因此,长效版格拉替雷Copaxone在全球主要市场的上市,将成为捍卫其MS专营权增加的重要筹码。仿制药格拉替雷注射剂是全球最畅销的多发性硬化症药物。然而,随着普通格拉替雷Copaxone专利到期,该药将会逐渐遭受廉价仿制药的冲击。2015年4月,诺华旗下仿制药企业山德士已成功开发仿制药Glatopa已于获FDA批准。该药是梯瓦(Teva)品牌药格拉替雷Copaxone的仿制药。Glatopa也是FDA批准的首个格拉替雷Copaxone仿制药,作为每日一次的注射药物,用于复发型多发性硬化症的治疗。Glatopa在美国由诺华山德士与Momenta合作开发,该药适用于复发型多发性硬化症(RMM)患者的治疗,也适用于经历过首次临床发作且核磁共振成像(MRI)所示特征表现与MS相符的患者。格拉替雷作为一个复杂的混合物仿制难度较大,目前,FDA已获得批准四家原料药生厂商的DMF文件,印度DrReddysLaboratoriesLtd.、美国AmbiopharmInc.、比利时PeptisynthaSa.和中国翰宇药业。随着专利到期也将会有更多企业参与到多发性硬化症药物市场的竞争。生物活性Glatirameracetate是髓鞘碱性蛋白的合成类似物和一种免疫调节剂,可用于多发性硬化症的研究。Glatirameracetate显示出与MHC分子强而杂乱的结合,因此与各种髓鞘抗原竞争,使其呈现给T细胞。Glatirameracetate作用的另一个方面是有效地诱导T辅助细胞2(Th2)的特异性抑制细胞迁移到大脑并导致原位旁观者抑制。体外研究Glatirameracetate(25-100mg/kg;S.c;5days)increaseBDNFlevels.Inhuntington’sdisease(HD)mousemodel,theN171-82Qtransgenicmouseline,whichexhibitsamorerapidlyprogressingdiseasecourse.Glatirameracetate(1mg/mouse;s.c.;5×week)beginningat8weeksofageandcontinuinguntil20weeksofage,whichisneartheageofdeathduetothedisease.Glatirameracetateelicitedimprovesperformanceonseveralmotorfunctionmeasures.GlatirameracetatesignificantlyimprovestheperformanceofN171-82Qtransgenicmiceat15weeksofageintherotarodtestmeasuredoverthecourseof4days. |
| 结构式: |
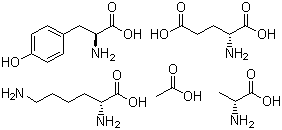 |
 |
|
声明:以上信息未经本网证实,仅供参考,华夏化工网不承担任何风险责任. |
|